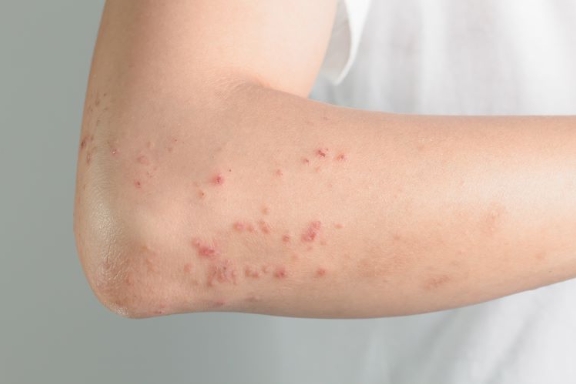
艾伯維(AbbVie)公布了特應性皮炎的首次頭對頭試驗的積極頂線結果,CPHI2024制藥原料展了解到試驗中評估了起始劑量為每天15mg的RINVOQ? (upadacitinib)與標示劑量的DUPIXENT?(dupilumab)。
IIIb/IV 期 LEVEL UP研究評估了對全身治療反應不足或不建議使用這些療法的患者,以及藥物在針對12 歲及以上患有中度至重度特應性皮炎的個體中的療效和安全性。
CPHI2024制藥原料展根據該研究的數據獲悉,中度至重度特應性皮炎患者,在經過治療后有望不再搔癢,皮膚上也不再有外傷。
喬治華盛頓大學醫學與健康科學學院皮膚病學教授兼臨床研究主任Jonathan Silverberg博士表示:“LEVEL UP研究的結果,利用upadacitinib等治療方案通過EASI 90和NRS 0/1的聯合測量來實現特應性皮炎的治療目標,而不僅僅是讓瘙癢減輕或皮膚清理,這很重要,因為很多患者的病情控制住了,但并未十分穩定。”
?
在LEVEL UP研究中,JAK抑制劑upadacitinib讓患者在第16周時濕疹面積和嚴重程度指數(EASI 90)和最嚴重瘙癢數評定量表0或1(WP-NRS 0/1),同時降低90%或更多(upadacitinib和dupilumab分別為19.9%和8.9%)。
?
此外,艾伯維(AbbVie)報告還表示,與度普利尤單抗相比,upadacitinib能夠快速實現皮膚清理,讓皮膚不再或偶爾瘙癢。
?
多數接受實驗的患者在第 16 周達到 EASI 90(40.8% 對 22.5%)
在第 16 周時實現 WP-NRS 為 0/1(30.2% vs 15.5%)。
艾伯維表示,在IIIb/IV期試驗中,upadacitinib的安全性與先前upadacitinib特應性皮炎臨床研究的安全性一致,LEVEL UP研究的這些結果未來將在醫學大會上公布。
CPHI2024制藥原料展基于分享行業資訊的目的轉載本文章,不代表我公司支持文中所述的觀點,也不為全文負責真實性,如有侵權,請及時聯系我們予以刪除。